Применение законов термодинамики
По просьбе нашего читателя постараемся описанную тему от 09:44 | 17.07.2016 раскрыть ещё глубже, сегодня рассмотрим Применение законов термодинамики. Не будем разливать воду, а преступим рассмотрению этого вопроса.
Основное положение
У правил термодинамики есть свой определенный предмет изучения и способ применения. Они с большой точностью описывают все макроскопические параметры изучаемых тел и дают заключение о функционировании тех или иных термодинамических систем. Однако все законы неспособны дать конкретных предположений, выраженных в точных математических формулировках. Подобные понятия принято изучать в другом разделе физики, который называется статистической физикой.
Рисунок 3. Третий закон термодинамики.
Все законы термодинамики не связаны между собой, поэтому и формируются по отдельным независимым группам. В процессе изучения удалось выяснить, что начала термодинамики не вытекают одно из другого и их нельзя в полной мере вывести в единое целое.
Любая термодинамическая система представляется в виде определенного числа параметров. Среди них можно найти внутреннюю энергию. Она формируется на основе кинетической энергии. Последняя энергия выступает в роли своеобразного строительного материала, из которого состоят все частицы системы. Внутренняя энергия может принимать любые фиксируемые очертания и иметь признаки:
- вращательного движения;
- колебательного движения;
- поступательного движения.
Энергия принимает формы потенциальной энергии, а также имеет основу кинетической энергии. Часто при расчетах идеальных газов сознательно уходят от потенциальной энергии. Внутренняя энергия часто называется функцией состояния термодинамической системы. Подобная функция определяется в качестве температуры газа, при этом значения внутренней энергии не будут лежать в зависимости от перехода в состояние. Это можно представить, как выход системы из первоначального состояния. В этом случае она подвергается определенным процессам и взаимодействию, проходит круг и возвращается в начальное состояние вновь.
Внутренняя энергия в подобных ситуациях будет равняться нулевому значению. Для идеального газа возможно изменить внутреннюю энергию. Это можно сделать двумя основными вариантами. При первом исследователи совершают работу при помощи газа. Второй способ предполагает сообщение нашей системе определенного количества теплоты. Таким образом, можно сформулировать первый закон термодинамики к тому, что количество теплоты, подведенное к термодинамической системе, будет расходоваться на совершение идеальным газом работы, осуществляемой механическим способом. Также меняется внутренняя энергия тела.
При рассмотрении второго начала термодинамики необходимо понимать, что для любой термодинамической системы характерно состояние равновесия. В этом состоянии все макроскопические величины во времени остаются на неизменном уровне, то есть объем, температура, давление параметра. В нашем случае, это идеальный газ. Состояние внутренней неизменности может строиться на ряде дополнительных условий:
- отсутствии теплопроводности;
- диффузии;
- химических реакций;
- иных условий.
Вывод системы из термодинамического равновесия при соблюдении всех условий предполагает ее возврат в первоначальное состояние. Главную роль в этом процессе играют внешние факторы. Все происходит по истечении определенного отрезка времени. При отсутствии названных внешних факторов происходит иная ситуация. Она может измениться самопроизвольным образом.
Замечание 2
В третьем начале термодинамики обсуждаются составные части любого процесса. Он может состоять из конечного числа циклов, при этом не достигаются внутри него температуры, близкие к абсолютному нулю.
При формировании нулевого или общего начала термодинамики установлено, что два тела, которые находятся в тепловом равновесии с другим телом, тоже могут находиться в тепловом равновесии между собой.
Определение 1
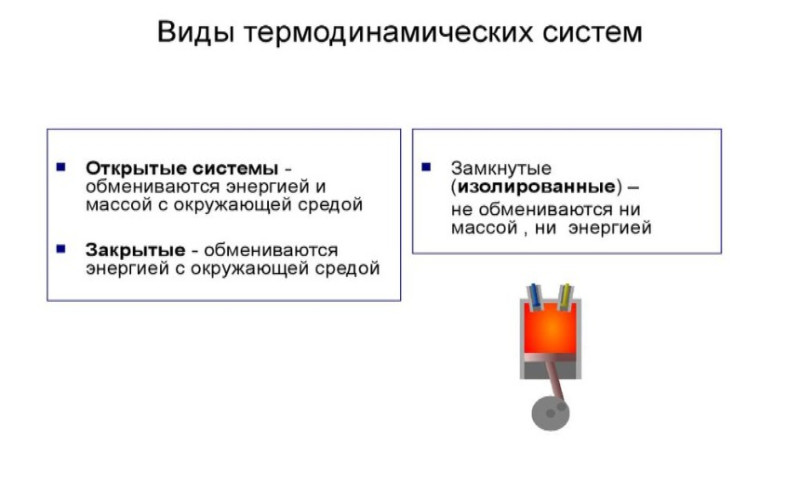
Рисунок 1. Виды термодинамических систем.
Живые системы считаются системами открытого типа и по этой причине будут относиться к неравновесным. Подобная термодинамически открытая система характеризуется тем, что в ней наблюдается постоянное протекание химических реакций. Биохимические реакции на каждой стадии в совокупности считаются каталитическими. Катализаторами в таких реакциях становятся белки-ферменты.
Живой организм способен получать пищу из внешней среды (и также - кислород, воду) и выделять в нее, наряду с тем, различные вещества. Теплообмен производится между организмом и средой. В таких условиях пребывает, например, космонавт внутри космического корабля. Его организм при этом является открытой по отношению к кораблю системой. В то же время, сам корабль является отлично изолированным от внешней среды.
Заключение
Конечно можно много говорить по теме Применение законов термодинамики, но основную суть мы изложили по этому вопросу. Если вам нужно дополнительная консультация, пожалуйста пишите ваши сообщения нам на почту. Все поступившие вопросы рассматриваются и не остаются без ответа.
ПОМОГАЕМ УЧИТЬСЯ НА ОТЛИЧНО!
Выполняем ученические работы любой сложности на заказ. Гарантируем низкие цены и высокое качество.
Деятельность компании в цифрах:
Зачтено оказывает услуги помощи студентам с 1999 года. За все время деятельности мы выполнили более 400 тысяч работ. Написанные нами работы все были успешно защищены и сданы. К настоящему моменту наши офисы работают в 40 городах.
РАЗДЕЛЫ САЙТА
Ответы на вопросы - в этот раздел попадают вопросы, которые задают нам посетители нашего сайта. Рубрику ведут эксперты различных научных отраслей.
Полезные статьи - раздел наполняется студенческой информацией, которая может помочь в сдаче экзаменов и сессий, а так же при написании различных учебных работ.
Красивые высказывания - цитаты, афоризмы, статусы для социальных сетей. Мы собрали полный сборник высказываний всех народов мира и отсортировали его по соответствующим рубрикам. Вы можете свободно поделиться любой цитатой с нашего сайта в социальных сетях без предварительного уведомления администрации.
ЗАДАТЬ ВОПРОС
НОВЫЕ СТАТЬИ
- Убыточность по операциям страхования жизни
- Убыточность по операциям, отличным от страхования жизни
- Относительный показатель страховой убыточности
- Сущность страховой убыточности
- Формы социальной защиты
ПОХОЖИЕ СТАТЬИ