Энтропийный метод анализа
По просьбе нашего читателя постараемся описанную тему от 07:37 | 11.04.2016 раскрыть ещё глубже, сегодня рассмотрим Энтропийный метод анализа. Не будем разливать воду, а преступим рассмотрению этого вопроса.
Основное положение
Чтобы перейти к энтропийному методу анализа необходимо уяснить, что каждый тепловой реальный процесс в термодинамике характеризуется ростом энтропии всей системы. Это же подразумевает второй закон термодинамики. Из этого следует, что в системе процесс приращения энтропии представляет собой общий абсолютный критерий, под которым подразумевается термодинамическое совершенство теплового процесса. Он характеризуется суммой приращения энтропии в локальном тепловом элементе. Это понятие связано с пропорциональностью перерасхода химической энергии топлива или иной подведенной энергии к изучаемому объекту. При анализе такого термодинамического метода формулируется задача в определении перерасхода топлива.
Также для аналитической термодинамики характерно использования некоторых иных методов:
- метод приращения эксергий;
- построение эксергетических диаграмм по методу приращений эксергетических тепловых потоков;
- вычисление эксергетического коэффициента теплопередачи.
Определение 1
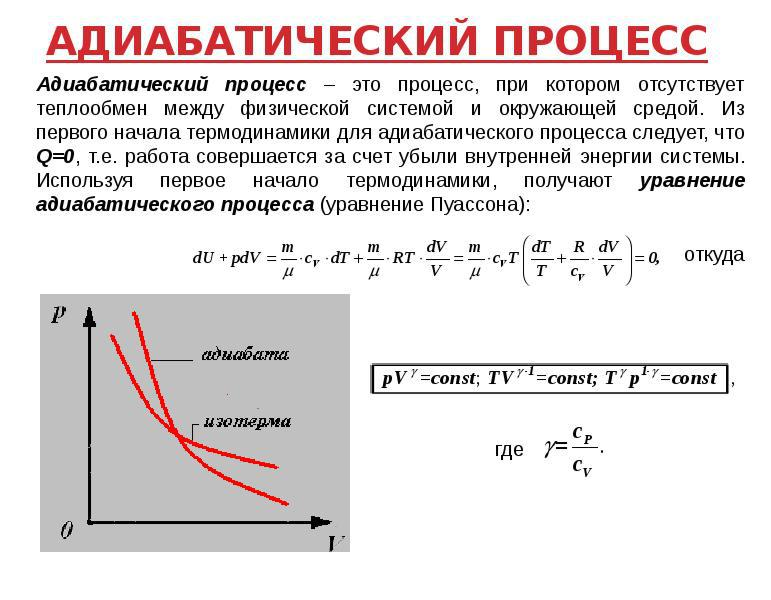
Рисунок 1. Адиабатический процесс.
Есть несколько основных факторов, которые характеризуют данный класс. Например, адиабатный процесс может происходит динамично и укладывается в достаточно короткий период времени. Происходят все адиабатные процессы в термодинамике, как правило, мгновенно.
Уравнение первого закона термодинамики для исследуемого класса имеет следующий вид: $du = -dl = -pdv$. Из этой формулы видно, что работа адиабатического процесса расширения совершается в результате постепенного уменьшения внутренней энергии идеального газа и, следовательно, температура самого элемента уменьшается. Работа адиабатного сжатия всегда идет на только увеличение внутреннего энергетического потенциала, то есть на повышение температурных параметров. Таким образом, изменения условий работы системы в адиабатном процессе эквивалентны по величине и противоположны по знаку.
В реальных условиях указанное термодинамическое явление возможно осуществить двумя методами:
- провести физический процесс так быстро, чтобы теплообмен не успел произойти;
- полностью изолировать систему от факторов внешней среды.
После введения в эксперименты вышеуказанных способов получаем такое уравнение: $dU + dA = 0$. Графически на координатной плоскости адиабатный процесс практически всегда изображается кривой, которая называется в физике адиабатой. Она падает намного круче, чем более постоянная изотерма, поскольку при этом явлении изменение давления происходит с помощью одновременного уменьшения температуры и увеличения объема.
Этот вывод теоретически подтверждает формула: $p = nkT$, ведь увеличение общего объема идеального газа ведет автоматически к уменьшению концентрации молекул изучаемого вещества, следовательно, уменьшение давления обусловливают два показателя — концентрация молекул $n$ и температура газа $T$.
Заключение
Конечно можно много говорить по теме Энтропийный метод анализа, но основную суть мы изложили по этому вопросу. Если вам нужно дополнительная консультация, пожалуйста пишите ваши сообщения нам на почту. Все поступившие вопросы рассматриваются и не остаются без ответа.
ПОМОГАЕМ УЧИТЬСЯ НА ОТЛИЧНО!
Выполняем ученические работы любой сложности на заказ. Гарантируем низкие цены и высокое качество.
Деятельность компании в цифрах:
Зачтено оказывает услуги помощи студентам с 1999 года. За все время деятельности мы выполнили более 400 тысяч работ. Написанные нами работы все были успешно защищены и сданы. К настоящему моменту наши офисы работают в 40 городах.
РАЗДЕЛЫ САЙТА
Ответы на вопросы - в этот раздел попадают вопросы, которые задают нам посетители нашего сайта. Рубрику ведут эксперты различных научных отраслей.
Полезные статьи - раздел наполняется студенческой информацией, которая может помочь в сдаче экзаменов и сессий, а так же при написании различных учебных работ.
Красивые высказывания - цитаты, афоризмы, статусы для социальных сетей. Мы собрали полный сборник высказываний всех народов мира и отсортировали его по соответствующим рубрикам. Вы можете свободно поделиться любой цитатой с нашего сайта в социальных сетях без предварительного уведомления администрации.
ЗАДАТЬ ВОПРОС
НОВЫЕ СТАТЬИ
- Убыточность по операциям страхования жизни
- Убыточность по операциям, отличным от страхования жизни
- Относительный показатель страховой убыточности
- Сущность страховой убыточности
- Формы социальной защиты
ПОХОЖИЕ СТАТЬИ